肉制品在生产和贮藏过程中会发生氧自由基积累并导致蛋白质氧化,降低了肉制品的质量和安全性。肌肉蛋白是肉蛋白的关键成分之一,其氧化稳定性对肉制品的功能品质具有重要影响。为提高肉制品的质量并延长其保质期,研究肌球蛋白在整个加工过程中发生的变化至关重要。蛋白质的特性可以通过与小分子的相互作用而改变。
茶黄素是一种具有羟基和苯甲酮结构的物质,存在于红茶中。茶黄素具有多种生理活性,如降低血液胆固醇和血糖水平、抗菌、抗炎和抗氧化。此外,茶黄素安全、无毒,在通过尿液和粪便排泄之前可以安全地被吸收。近年来,越来越多的研究人员将茶多酚化合物应用于肌纤维蛋白的修饰。然而这些研究主要集中于茶多酚对蛋白质结构和功能的整体影响,而很少研究茶多酚对具体蛋白质的影响。
陕西师范大学食品工程与营养科学学院学院的Liu Guanxu等为确定茶黄素对牛肌球蛋白的结构和功能特性影响,使用光谱学和分子动力学研究两者之间的相互作用,并通过体外消化实验确定复合物的消化特性,以证实茶黄素在肉蛋白系统中的潜在应用。

图1 肌球蛋白(0.5 mg/mL)在不同茶黄素添加量下的紫外-可见吸收光谱
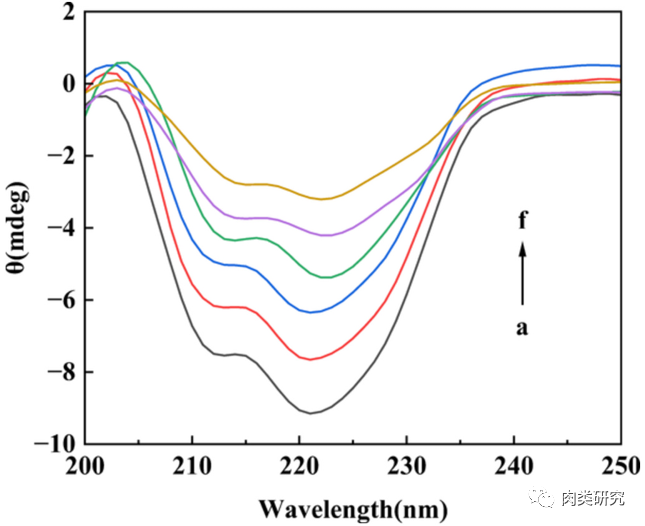
(a)0 mg/mL;(b)0.01 mg/mL;(c)0.02 mg/mL;(d)0.03 mg/mL;(e)0.04 mg/mL;(f)0.05 mg/mL。
图2 肌球蛋白(0.3 mg/mL)与不同含量茶黄素的圆二色光谱
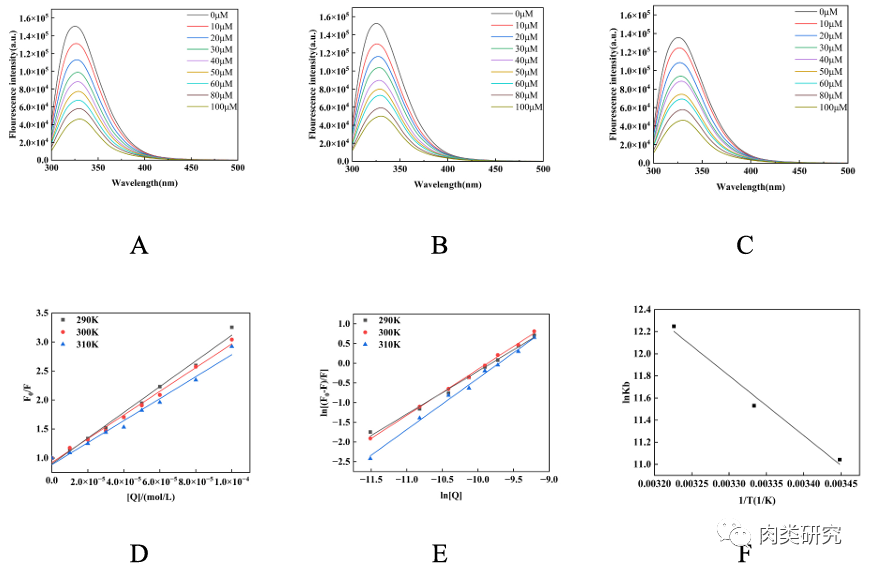
(A)290 K;(B)300 K;(C)310 K;(D)牛肌球蛋白猝灭牛肌球蛋白的Stern-Volmer曲线;(E)茶黄素与牛肌球蛋白相互作用的双对数曲线;(F)不同温度下茶黄素和牛肌球蛋白相互作用的热力学参数。
使用荧光和紫外-可见光光谱表征在有或没有茶黄素的情况下蛋白质的变化,发现茶黄素与肌球蛋白之间形成了复合物,茶黄素与肌球蛋白的相互作用和结构修饰提高了肌球蛋白的溶解度,同时降低了表面疏水性,影响肌球蛋白的微环境。温度升高有利于茶黄素与牛肌球蛋白的结合。这种相互作用导致肌球蛋白的α-螺旋含量降低。对荧光猝灭机制的进一步研究发现,复合物通过静态猝灭形成,并具有良好的稳定性。

图4 (A)最低结合亲和力(-125.35 kJ/mol)茶黄素和肌球蛋白的对接模型;(B)黄素和肌球蛋白之间的二维相互作用示意图
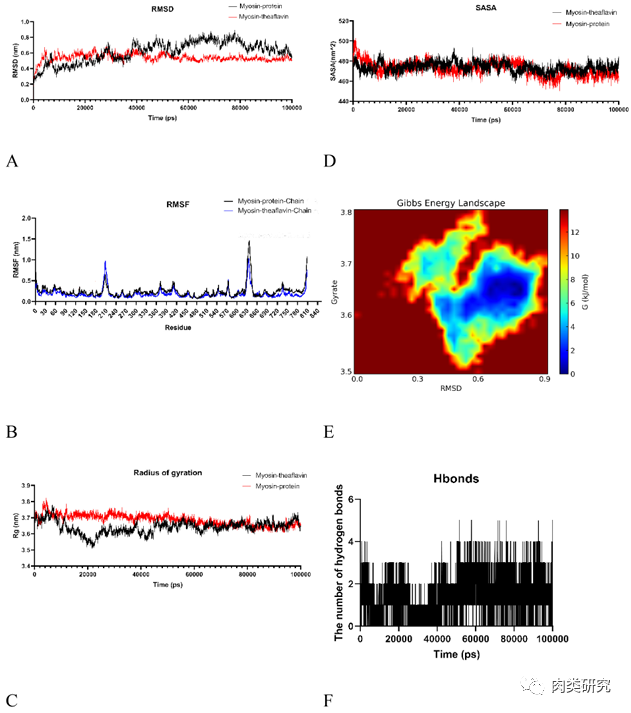
(A)均方根偏差(RMSD);(B)回转半径(R
g
);(C)均方根波动(RMSF);(D)SASA分析;(E)吉布斯自由能形貌图;(F)模拟时间内复合物中氢键的数量。
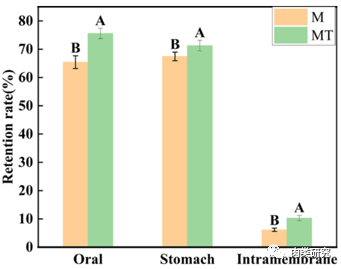
蛋白质和复合物的分子对接模拟揭示了黄素和肌球蛋白之间的联系,与茶黄素结合后,疏水相互作用和氢键使蛋白质结构更紧凑,蛋白质稳定性显著提高。茶黄素以最小的结合亲和力成功地与蛋白质相互作用(-125.35 kJ/mol)。在MD模拟中,氢键和疏水相互作用显示支持复合物的生长和稳定性。体外消化实验结果表明,在消化过程中加入茶黄素可显著降低肌球蛋白的消化率。
以上研究结果表明,在肉类蛋白系统中添加黄酮类物质,可以改善蛋白质在加工过程中的性质变化,增强其对人体的益处(减少肉制品食用过程中血糖浓度的增加),并开发新的功能性食品。
文章《Molecular dynamics simulation and in vitro digestion to examine the impact of theaflavin on the digestibility and structural properties of myosin》发表于International Journal of Biological Macromolecules 2023年247卷
新闻转载地址:https://mp.weixin.qq.com/s/F7X8CrzG-3D1f7HGzlzxpA